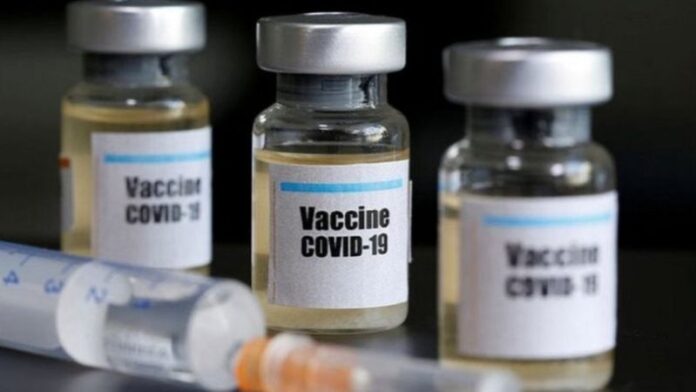
ANTARA/REUTERS/DADO RUVIC/PRI
JIC, — Pelaksanaan uji klinis vaksin Covid-19 Sinovac tahap tiga dapat dilakukan setelah Komite Etik Penelitian Universitas Padjajaran (Unpad), Bandung, memberikan persetujuan.
“Benar, (Komite Etik) sudah (menyetujui),” ujar Ketua tim riset uji klinis vaksin Covid-19 Unpad, Profesor Kusnandi Rusmil, sebagaimana dilansir situs resmi Unpad pada Senin (27/07).
Selanjutnya, tim riset uji klinis vaksin Covid-19 Unpad mulai membuka pendaftaran peserta terhitung mulai Senin (27/7).
Pada Jumat (24/07), Kusnandi mengatakan rekomendasi dari Komite Etik Penelitian Universitas Padjajaran diperlukan karena “ingin memastikan keselamatan relawan”.
Ia mengungkapkan, komite etik meminta sejumlah perbaikan dalam hal prosedur pengujian vaksin agar lebih memastikan keselamatan para relawan.
“Ada tambahan pemeriksaan yang diminta. Kenapa diminta? Karena ini penyakit baru sehingga perlu hati-hati jangan sampai ada apa-apa. Mungkin pemikirannya seperti itu dari komite etik. Pada prinsipnya agar subyek (relawan), aman,” kata Prof. Kusnandi, seperti dilaporkan wartawan di Bandung, Yuli Saputra, untuk BBC News Indonesia.
SUMBER GAMBAR,REUTERS
Apa kriteria untuk menjadi calon peserta?
Prof. Kusnandi menjelaskan, ada sejumlah kriteria yang harus dipenuhi calon peserta uji klinis.
Pertama, calon peserta merupakan orang dewasa berusia antara 18 – 59 tahun yang dinyatakan sehat, serta senantiasa mematuhi protokol kesehatan dan melakukan pembatasan fisik maupun sosial selama wabah pandemi Covid-19 berlangsung. Calon peserta juga dinyatakan tidak memiliki riwayat terinfeksi virus corona.
“Calon peserta akan dilakukan tes terhadap apus tenggorokan (swab test) dan rapid test untuk mengetahui apakah ada kemungkinan sedang atau pernah terinfeksi Covid-19,” jelasnya, dalam situs resmi Unpad.
Ia menegaskan, peserta akan mendapatkan tes swab maupun tes rapid secara cuma-cuma.
Sehat atau tidaknya kondisi calon peserta dibuktikan dengan tidak mengalami penyakit ringan, sedang, atau berat serta tidak memiliki riwayat penyakit asma dan alergi terhadap vaksin.
Calon peserta juga tidak memiliki kelainan atau penyakit kronis seperti gangguan jantung, tekanan darah tinggi yang tidak terkontrol, diabetes, penyakit ginjal dan hati, tumor, epilepsi atau penyakit gangguan syaraf lainnya.
Lebih lanjut Prof. Kusnandi menjelaskan, calon peserta tidak memiliki kelainan darah atau riwayat pembekuan darah, tidak memiliki penyakit infeksi lain dan demam, serta tidak memiliki riwayat penyakit gangguan sistem imun. Suhu tubuh calon pendaftar juga tidak boleh melebihi 37,5 derajat Celcius.
Selanjutnya, calon peserta bukan merupakan perempuan hamil atau berencana hamil selama periode penelitian, serta tidak sedang menyusui. Calon peserta juga tidak sedang ikut atau akan diikutsertakan dalam uji klinis lain.
“Peserta tidak mendapat imunisasi apa pun dalam waktu 1 bulan ke belakang atau akan menerima vaksin lain dalam satu bulan ke depan,” tutur Prof. Kusnandi.
Calon peserta berdomisili di Kota Bandung dan tidak berencana pindah dari lokasi penelitian sebelum penelitian selesai dilaksanakan.
Prof. Kusnandi menegaskan, dalam 14 hari sebelum dimulainya penelitian, peserta tidak memiliki riwayat kontak dengan pasien terinfeksi virus corona, tidak memiliki riwayat kontak dengan pasien yang menunjukkan demam atau gejala sakit saluran pernapasan yang berdomisili di daerah atau komunitas yang terdampak Covid-19, serta tidak memiliki dua atau lebih kasus demam dan/atau gejala saluran pernapasan di daerah dengan lingkup kecil, seperti rumah, kantor, dan sekolah.
Berapa banyak calon peserta yang diperlukan?
Sebanyak 1.620 relawan dibutuhkan dalam proses uji klinis vaksin. Namun, tidak semua peserta akan disuntikkan vaksin.
Sebanyak 540 orang akan disuntikkan vaksin, sedangkan sisanya akan mendapat cairan plasebo. Penentuan pemberian vaksin atau plasebo akan dilakukan secara acak.
“Bagi yang menerima plasebo akan mendapatkan vaksin Covid-19 setelah vaksin didaftarkan,” jelas Prof. Kusnandi.
Kesehatan peserta dipastikan tetap dipantau oleh petugas penelitian secara tertatur selama jalannya penelitian, atau sekitar enam bulan setelah pemberian vaksin terakhir.
Prof. Kusnandi memastikan, seluruh peserta dilindungi asuransi kesehatan.
Pendaftaran peserta uji klinis dibuka hingga 31 Agustus 2020.
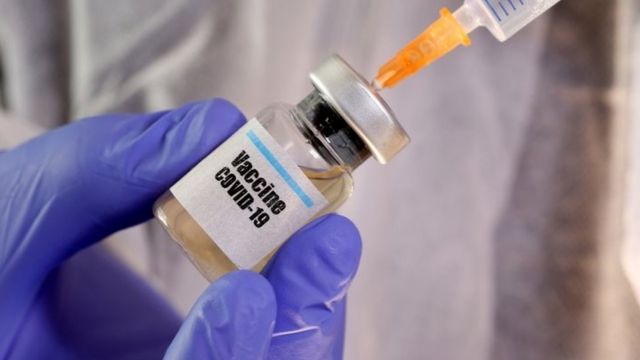
SUMBER GAMBAR,REUTERS
Pemerintah ‘menjamin kesehatan’ para relawan
Sementara itu, pemerintah Indonesia melalui Satuan Tugas Penanganan COVID-19 mengatakan mereka berkomitmen melindungi kesehatan para relawan.
“Jaminan kesehatan, semua pasti akan dilindungi pemerintah. Kami update kalau keadaan sudah semakin jelas,” ujar Juru Bicara Satuan Tugas Penanganan COVID-19, Wiku Adisasmito (24/07).
Sebelumnya, uji klinis vaksin Covid 19 ditargetkan akan dilakukan awal Agustus 2020, namun proses itu masih menunggu rekomendasi Komite Etik.
Rekomendasi itu diperlukan untuk diajukan ke Badan POM, sebagai pihak yang berwenang untuk mengeluarkan izin uji klinis vaksin.
“Fase tiga untuk lebih memastikan vaksin ini aman dan mempunyai efek yang baik (menimbulkan antibodi) dengan jumlah sampel di banyak tempat,” kata Kusnandi, yang merupakan salah satu ahli vaksin di Indonesia ini.
Uji klinis Sinovac
Di Indonesia, uji klinis Sinovac dilakukan kerjasama antara Unpad dan Biofarma, di enam lokasi di Kota Bandung, yakni di Rumah Sakit Pendidikan Unpad, Balai Kesehatan Unpad, dan empat puskesmas.
Berdasarkan hitungan statistik yang dilakukan Biofarma, dibutuhkan sebanyak 1.620 relawan yang berusia antara 18 hingga 59 tahun.
“Kenapa usia produktif yang jadi target? Karena mereka bisa bekerja dengan baik, sehingga negara tidak defisit,” kata Kusnandi.

SUMBER GAMBAR,YULI SAPUTRA UNTUK BBC NEWS INDONESIA
Uji klinis ini juga melibatkan sejumlah tim yang beranggotakan dokter anak, dokter penyakit dalam, dan orang dengan keahlian yang dibutuhkan.
Dalam proses penelitian ini, koordiinator lapangan tim uji klinis vaksin Covid 19, Eddy Fadlyana mengatakan, 1.620 relawan akan dibagi dua kelompok besar, masing-masing 810 orang.
Satu kelompok akan disuntikan vaksin, satu lagi hanya disuntikan cairan H2O, untuk menguji efek plasebo.
Untuk memenuhi standar registrasi vaksin, 540 orang pertama yang divaksin akan dipantau selama tiga bulan untuk melihat keamanan dan efektivitas vaksin.
“Setelah tiga bulan dipantau, pemantauan akan dilanjutkan selama tiga bulan berikutnya, terutama untuk efikasinya (efektivitasnya).
“(Membandingkan) mereka yang dapat plasebo dengan yang mendapat vaksin apakah angka risiko sakitnya sama, rendah atau lebih tinggi selama 6 bulan itu.
“Maka kita mendapat data yang lengkap setelah enam bulan. Kekebalan setelah enam bulan dipantau lagi, apakah kekebalannya masih cukup tinggi sehingga kekebalan lebih panjang atau sudah turun,” ujar Eddy.
Selain Indonesia, uji klinis Sinovac dilakukan di Brasil, India, Bangladesh, dan Chili.
“Kalau umpamanya di lima negara ini dijadikan satu dan hasilnya aman, maka vaksin ini boleh dijual,” kata Ketua Tim Uji Klinis Vaksin Fakultas Kedokteran Unpad, Kusnandi Rusmil Kusnandi.
Klaim keamanan vaksin juga didasarkan pada bahan vaksin yang menggunakan virus SAR Cov2 yang dimatikan, bukan dilemahkan.
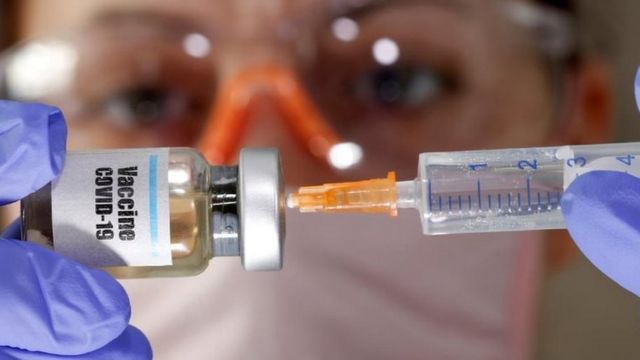
SUMBER GAMBAR,REUTERS/DADO RUVIC/ILLUSTRATION
‘Sesuai dan cocok’
Juru Bicara Satuan Tugas Penanganan COVID-19, Wiku Adisasmito dalam konferensi pers (24/07) mengatakan pemerintah berusaha mencari vaksin yang sesuai dan cocok untuk masyarakat Indonesia.
Pemerintah, ujar Wiku, memprioritaskan tiga hal, ujarnya, yakni keamanan, ketepatan, dan kecepatan.
Dari aspek keamanan, ia mengatakan, vaksin harus mampu memberi perlindungan dan tak memiliki efek samping.
“Harus tepat artinya, betul-betul vaksin tersebut harus bisa menimbulkan kekebalan spesifik pada virus yang beredar di Indonesia,” ujarnya menjelaskan aspek ketepatan.
Sebelumnya Prof Wasito, yang terlibat dalam penelitian dan pengujian vaksin pada hewan untuk penyakit yang disebabkan oleh virus corona di Michigan State University, Amerika Serikat selama kurang lebih 12 tahun, mengatakan galur atau strain virus corona yang ada di Indonesia mungkin berbeda dengan galur virus corona di negara lain.
Maka itu, kata Warsito, jenisnya harus dipastikan terlebih dahulu agar vaksin virus corona dapat bekerja dengan efektif.
“Cara terbaiknya adalah kita harus menentukan galur-galur virus corona yang ada di seluruh Indonesia. Kemudian kita bisa menentukan apakah sequenceDNAvirus kita sama dengan yang di China atau di AS. Kalau itu beda sama sekali, kita harus membuat vaksin sendiri.
“Kita tidak bisa mengandalkan vaksin dari luar negeri, karena misalnya urutan DNA [virus corona di luar negeri] itu berbeda dengan DNA virus corona yang ada di Indonesia,” ujarnya.
Menjawab kekhawatiran itu dan kemungkinan mutasi virus, Ketua Tim Uji Klinis Vaksin Fakultas Kedokteran Unpad, Kusnandi Rusmil meminta masyarakat tak usah khawatir.
“Yang disebut mutasi itu kan berubah ya. Tapi berubahnya nggak langsung. Umpanyanya ini burung, tau-tau jadi kucing. Ya nggak begitu, cuma [misalnya], ada yang tambah gemuk, ada yang tambah kecil.
“Sehingga kalaun diimuniasi macam kuman apa pun sama vaksinnya. Jadi kita nggak usah terlalu memikirkan mutasi-mutasi itu,” kata Kusnandi.
Ia memberi contoh vaksin Bio Farma yang diekspor ke 132 negara dan tidak dipermasalahkan.
‘Kalau ada mutasi itu sedikit tapi itu ter-cover oleh vaksin.”

SUMBER GAMBAR,JAKUB PORZYCKI/NURPHOTO VIA GETTY IMAGES
‘Pertandingan kecepatan’
Sementara itu untuk aspek kecepatan, pemerintah mengatakan tak hanya cepat, uji klinis vaksin harus dilakukan dengan benar dan bisa diproduksi dalam jumlah memadai bagi seluruh rakyat Indonesia.
Sebelumnya, dalam pertemuan dengan Jokowi, Koordinator Uji Klinis Vaksin Covid-19 yang juga Ketua Tim Riset Kusnandi Rusmil mengatakan, presiden meminta pihaknya menghasilkan vaksin dalam waktu tiga bulan.
Namun, Kusnandi mengatakan hal itu tak mungkin karena mereka ‘harus melakukan dengan hati-hati dan dengan benar’.
Selain bekerja sama dengan perusahaan China Sinovac untuk memproduksi vaksin Covid-19, pemerintah mengatakan mereka menggandeng institusi dalam negeri untuk ‘berlomba’ menghasilkan vaksin.
Hal itu dijelaskan Juru Bicara Satuan Tugas Penanganan COVID-19, Wiku Adisasmito, dalam konferensi pers Jumat (24/07).
Wiku mengatakan, selain Sinovac yang bekerja sama dengan BUMN Bio Farma, ada konsorsium lain yang tengah berusaha menghasilkan vaksin virus corona.
Salah satunya, kata Wiku, adalah konsorsium Eijkman, Kemenristek Brin, dan Bio Farma.
Ia juga menyebut ada rencana untuk menggandeng pihak swasta, yakni perusahaan farmasi Kalbe Farma.
“Bahwa apapun kerjasamanya, produksinya dengan perusahaan dalam negeri. Ini adalah suatu pertandingan kecepatan… Maka dari itu, siapa pun yang terbaik di Indonesia mari kita berlomba dan menjalankan dengan baik.
“Mohon para pakar, para ahli, dan lembaga untuk infklusif. Mari kita gunakan sumber daya nasional, keahlian yang ada di Indonesia dengan baik,” kata Wiku.
Hingga Kamis (23/07), jumlah kasus positif Covid-19 di Indonesia mencapai lebih dari 93.000 dan 4.500 kematian.
(Berita ini diperbarui sekitar pukul 13.45 WIB, Jumat (24/07), dengan menambahkan hasil keterangan pers Tim Uji Klinis Vaksin Fakultas Kedokteran Unpad, Bandung)
Sumber : bbcindonesia.com